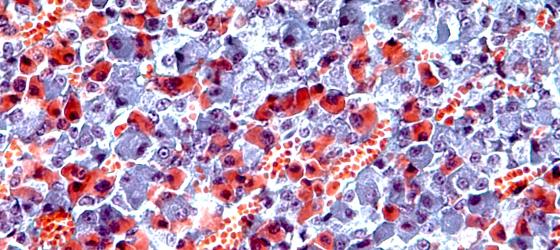
I tessuti sono composti da cellule di forma e funzione differente. La variazione di struttura delle singole cellule e la loro disposizione spaziale può indicare se i tessuti sono soggetti ai processi di normale trasformazione fisiologica oppure a variazioni che possono indicare la presenza di eventuali patologie.
Un esame microscopico sufficientemente accurato può evidenziare la presenza e l’evolversi di tali processi e indicare le variazioni istologiche e funzionali di tessuti o organi.
Per ottenere un buon preparato istologico il tessuto da esaminare deve essere sottoposto, operando con estrema cura, ai seguenti passaggi di preparazione:
- fissazione
- inclusione
- taglio
- colorazione
- visione al microscopio
1. Fissazione. Il primo trattamento a cui un tessuto deve essere sottoposto,dopo essere stato prelevato in vivo tramite biopsia o da cadavere in sede autoptica, è la fissazione. La fissazione è una procedura molto delicata da cui dipende la conservazione dell’organizzazione della cellula, dei componenti tissutali dei vari tessuti e, di conseguenza, la possibilità di una loro disamina.
Lo scopo della fissazione è quello di uccidere rapidamente le cellule dei tessuti mediante processi chimici o fisici che, nel più breve tempo possibile, inattivano l’azione di enzimi e batteri litici al fine di evitare la disorganizzazione della cellula e del tessuto.
I fissativi possono essere primari, cioè formati da un unico componente (es. formalina, acido picrico, tetrossido di osmio) o essere miscele di composti diversi (es. Bouin, Zenker, Susa) che, sfruttando le diverse caratteristiche dei componenti (come velocità di penetrazione, azione di decalcificazione, affinità per determinati coloranti), possono avere un’azione fissante più adatta agli scopi prefissati. Questi composti vengono detti denaturanti quando operano una sorta di coagulazione delle proteine presenti nel tessuto (es. etanolo, acido picrico, cloruro mercurico), o non coagulanti quando agiscono mediante la gelificazione dei vari componenti tissutali, (es. formalina, tetrossido di osmio). I fissativi chimici più usati sono generalmente la paraformaldeide al 2,5% e le miscele di Buoin, di Zenker e di Carnoy. Molte volte, alla fissazione chimica viene associata anche la fissazione fisica, per cui il processo di fissazione avviene nel frigorifero o nel freezer. Quando si vuole una risposta molto veloce, per esempio in sala operatoria, o quando si deve assolutamente evitare la denaturazione delle proteine cellulari, si deve fissare tramite congelamento a -80°C con metil butano e azoto liquido e includendo in una resina particolare, l’OCT. Il campione così trattato viene conservato in congelatore a -80°C e poi sezionato al criostato.
2. Inclusione. Con il processo detto inclusione i pezzi anatomici vengono racchiusi in un mezzo indurente il più possibile inerte per poter essere conservati e tagliati in sezioni più o meno sottili. Vi sono molti mezzi includenti a disposizione che vanno scelti volta per volta in base ai metodi di indagine a cui si ricorrerà successivamente. Un parametro molto importante per la scelta del mezzo di inclusione è lo spessore delle sezioni di tessuto che si vogliono ottenere. Se si vogliono ottenere delle sezioni semifini, cioè dello spessore di 1-1,5 µm, si include in resine come il glicolmetacrilato (GMA) o il metilmetacrilato (MMA). Se invece abbiamo bisogno di sezioni con spessore dai 3 ai 25 µm l’inclusione viene effettuata utilizzando miscele diverse di paraffine. La scelta delle varie miscele di paraffine, che vanno da un punto di fusione di 50-52°C a uno di 60-62°C, dipende dalle condizioni ambientali, dal tessuto esaminato, dalle sue dimensioni e dal suo grado di durezza. Di norma più un campione è duro e grande più deve essere dura la miscela di paraffine da usare. Infine, se lo studio del campione prevede marcature in immunofluorescenza si utilizza l’OCT, una resina plastica che solidifica a basse temperature.
3. Taglio. I blocchetti così preparati devono essere tagliati in sezioni di spessore opportuno per essere poi colorate e analizzate al microscopio. La scelta dello strumento di taglio dipende sia dallo spessore che si vuole ottenere che dal tipo di inclusione utilizzato. Per ottenere sezioni semifini si usa l’ultramicrotomo, una speciale versione del microtomo che monta particolari lame in acciaio o diamante. Per sezioni che vanno dai 3 ai 25 µm si utilizza il microtomo, strumento che permette lo scivolamento del blocchetto di inclusione su di una lama. Il taglio sarà effettuato con microtomi rotativi quando i pezzi hanno una dimensione relativamente piccola e taglio sottile (4 - 12 µm), con microtomi a slitta se si tratta di campioni di dimensione e spessore notevoli. Se invece l’inclusione è stata fatta utilizzando OCT si utilizza il criostato, una sorta di microtomo alloggiato in un contenitore refrigerato a -20, -40°C, che permette di ottenere sezioni che vanno dai 5 ai 20 µm.
4. Colorazione. Con il termine colorazione si indica quel processo in cui le sezioni di tessuto depositate su vetrino vengono fatte reagire con composti diversi che si legano alle componenti del tessuto stesso dando loro una colorazione caratteristica che permette di analizzarne la morfologia. Nel corso del tempo sono stati individuati coloranti con caratteristiche diverse (differente colore e/o affinità di reazione) che, anche in combinazione, permettono di analizzare al meglio la morfologia dei vari tessuti. Per ottimizzare le varie metodiche, sono state messe a punto diverse tecniche di colorazione:
- le colorazioni istologiche, in cui si usano uno o più coloranti che permettono l’analisi della morfologia del tessuto;
- le colorazioni istochimiche, in cui si usano composti chimici che reagiscono con componenti specifiche del tessuto. La reazione chimica derivante darà un precipitato colorato direttamente sulla sezione;
- le colorazioni immunoistochimiche, in cui si usano anticorpi per marcare componenti specifiche del tessuto. Questa tipo di colorazione è altamente selettiva perchè utilizza la specificità di reazione tra anticorpo e antigene (eventualmente presente nel tessuto);
- le colorazioni in immunofluorescenza, sono una variante di quelle immunoistochimiche e in cui si usano anticorpi secondari legati a fluorocromi che emettono, dopo eccitazione, un segnale luminoso con lunghezze d’onda caratteristiche e rilevabili con un microscopio a fluorescenza o confocale.
5. Visione al microscopio. Per fare una diagnosi e dotarla della relativa documentazione fotografica dobbiamo, oltre ad avere una buona conoscenza teorica dei tessuti, saper usare correttamente il nostro strumento di indagine: il microscopio ottico.
Il microscopio ottico è dotato di:
- stativo,
- oculari,
- obiettivi,
- viti macrometriche e micrometriche.
Il buon uso di questi componenti ci permetterà di sfruttare al massimo le potenzialità di questo strumento.
Una volta seduti al microscopio vanno eseguite le seguenti operazioni:
- si regolano gli oculari, della potenza standard d’ingrandimento di 10x, alla propria distanza inter-pupillare mediante un allargamento o avvicinamento degli stessi,
- si regola la luce, che non deve mai essere troppo forte, con il potenziometro
- si pone il vetrino sul tavolino portaoggetti e si mette a fuoco con l’obiettivo più piccolo. Solitamente nel revolver portaobiettivi sono presenti 5 obiettivi: il 4x, il 10x, il 20x, il 40x, il 100x. E‘ importante iniziare la visione con l’obiettivo a più basso ingrandimento proprio per avere un’immagine generale del preparato, della colorazione e delle condizioni di conservazione.
Una volte effettuate le diverse regolazioni si passa alla visione del preparato seguendo i seguenti accorgimenti:
- la visione deve iniziare dal margine libero del preparato, connettivo capsulare o epitelio di rivestimento che sia, così da poter avere una visione chiara e ordinata dei tessuti (negli organi pieni per margine libero si intende la parte più esterna, normalmente rivestita da una capsula connettivale mentre per gli organi cavi si intende la superficie interna della cavità, rivestita da epitelio; se l’organo del preparato è molto grande, come ad esempio fegato, milza o polmone, il margine libero può non essere apprezzabile)
- dopo una prima disamina a piccolo ingrandimento si possono usare gli altri ingrandimenti (ad es. 20x o 40x) in modo da confermare in maniera più accurata la diagnosi
- quando si guarda uno striscio di sangue, di espettorato polmonare o di spermatozoi si deve usare, per avere una visione sufficientemente ingrandita delle cellule, almeno il 40x
- tenere presente che per ottenere l’ingrandimento definitivo bisogna moltiplicare la risoluzione dell’oculare (sempre 10x) per quella dei vari obiettivi: quindi osservando con l’obiettivo 4 si avrà un preparato ingrandito di 40 volte (ingrandimento 10 dell’oculare moltiplicato per 4 ingrandimento dell’obbiettivo = ingrandimento 40X). Se osserviamo con obiettivo 10 avremo 100 ingrandimenti e cosi via. Per comodità la parola ingrandimento viene sostituita dalla sigla x così avremo preparati osservati a 40x,100x, 200x, ecc.